국내연구진 암세포에만 결합하는 단백질-금 소재 고안
광열치료 '나노독성'·'체외배출' 한계 극복
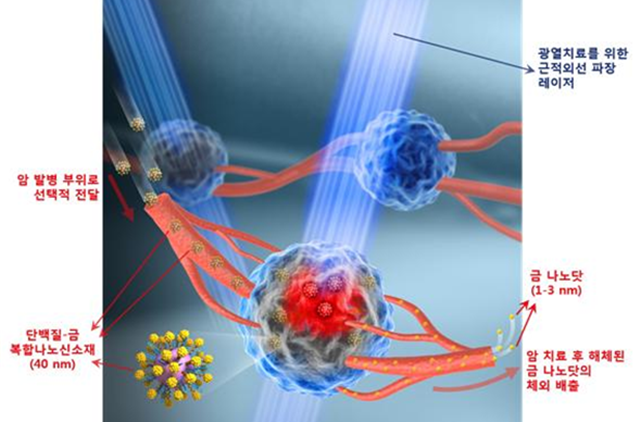
국내 연구진이 암세포에만 결합하는 펩타이드와 금을 결합시킨 나노신소재를 개발했다. 이를 통해 레이저를 이용해 암세포를 치료하는 광열치료의 항암효과와 안전성을 높일 수 있을 것으로 기대를 모으고 있다.
이지원 고려대 교수와 김광명 KIST 박사팀은 단백질 나노입자 표면에 암세포 특이적으로 달라붙는 펩타이드와 직경 3나노미터(㎚) 이하 초미세 금 나노입자가 동시에 결합돼 존재하는 '단백질-금 복합 나노신소재'를 개발했다고 9일 밝혔다.

이에 연구팀은 정상세포가 아닌 암세포에만 결합할 수 있도록 인도하는 표적 펩타이드와 체외로 배출되기 쉬운 초미세 금 나노입자를 결합했고, 이 소재를 이용해 생쥐의 정맥에 주사한 결과 기존의 금 나노입자에 비해 암 발병부위로의 전달이 훨씬 효과적으로 이뤄짐을 확인했다.
인간 유방암 세포로 종양을 유도한 생쥐에 개발된 나노신소재를 이용, 근적외선 광열치료를 한 결과에서도 암세포가 괴사됐고, 이후 3주간 생쥐의 장기와 조직을 살펴본 결과 금 나노입자가 잔존하지 않았다.
이 교수는 "개발된 단백질-금 복합 나노신소재로 암 발병 부위로 선택적 전달 효능을 향상시켜 광열치료 효과를 극대화하는 한편 기존 금 나노입자의 체내축적으로 인한 장기·조직 문제를 해결할 수 있는 실마리가 될 것"이라고 밝혔다.
한편, 이번 연구는 미래창조과학부가 추진하는 중견연구자지원사업과 선도연구센터지원사업의 지원으로 수행됐고 첨단재료 분야 국제학술지 '어드밴스드 머티리얼스지' 7월 8일자에 게재됐다.
댓글 정렬