글 : 김호민 IBS 바이오분자 및 세포구조 연구단
'가짜 스파이크단백질·수용체'로 치료
| IBS(기초과학연구원)는 코로나바이러스감염증-19(코로나19)와 코로나19의 원인인 사스-코로나바이러스-2(SARS-CoV-2 또는 2019-nCoV)에 대한 과학 지식과 최신연구 동향을 담은 <코로나19 과학 리포트>를 발행합니다. IBS 과학자들이 국내외 최신 연구동향과 과학적 이슈, 신종 바이러스 예방·진단·치료에 도움이 될 만한 연구진행 상황과 아이디어 등을 시민들과 공유하고자 합니다. <코로나19 과학 리포트 바로가기> |
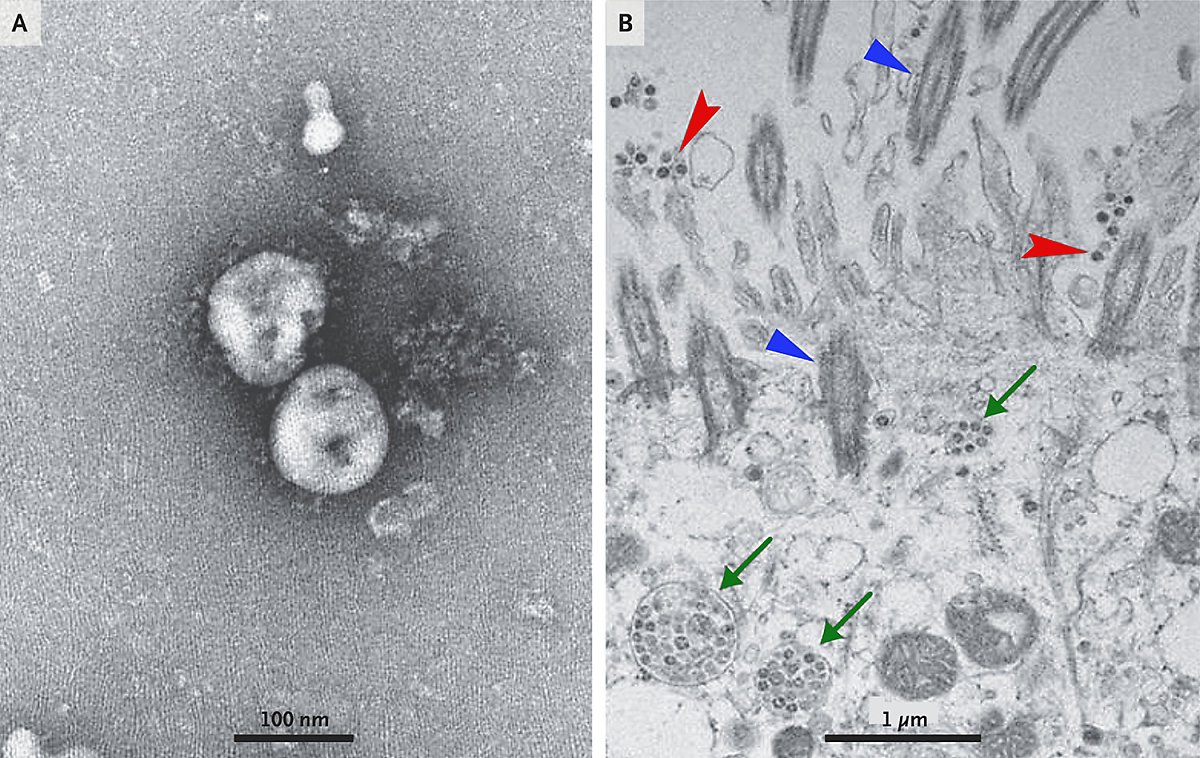
2019년 12월 하순. 중국 우한지역에서 원인불명 폐렴환자들이 늘어남에 따라 중국 질병예방통제센터(CCDC)와 의료진, 그리고 과학자들은 신속하게 신종 질병 대응연구팀을 구성했다. 대응팀은 환자의 기관지 폐포 세척액을 분석해 신종 코로나바이러스(2019-nCoV 또는 SARS-CoV-2)를 발견하고, 전자현미경 사진과 해독한 2019-nCoV의 유전체 서열 전체를 학계에 빠르게 발표했다(Lu et al., 2020; Wu et al., 2020; Zhou et al., 2020; Zhu et al., 2020). 최초 확진자가 발생한지 불과 한 달만의 일로, 이를 토대로 전 세계 과학자들이 많은 연구결과를 내놓고 있다.
◆ 스파이크단백질과 단백질가위 합작으로 침투
코로나바이러스를 투과전자현미경(TEM)으로 관찰하면, 바이러스 막 바깥쪽 표면에 돌기형태의 단백질(스파이크단백질)이 촘촘히 달려있는 구조를 볼 수 있다. 그 형태가 태양의 코로나와 비슷해 코로나바이러스라는 이름이 붙었다. 축구화 밑바닥의 스파이크가 미끄러짐을 방지하는 것처럼, 스파이크단백질은 숙주세포와 강하게 결합하여 바이러스가 숙주세포로 빠르게 침투하도록 지지해준다.
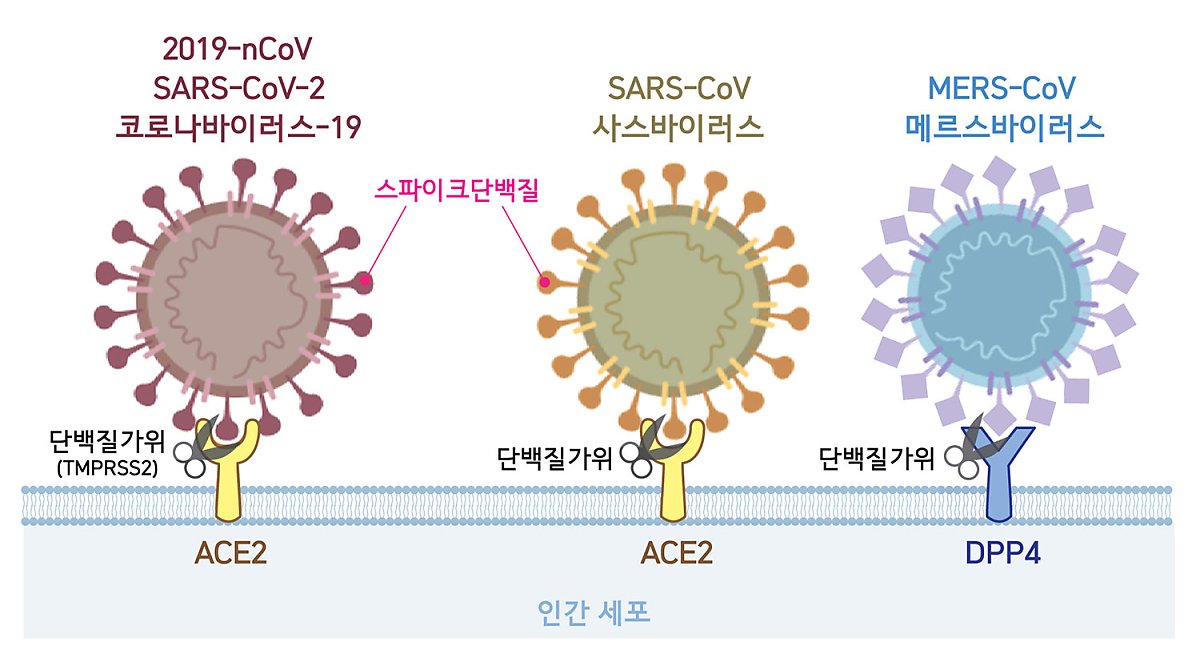
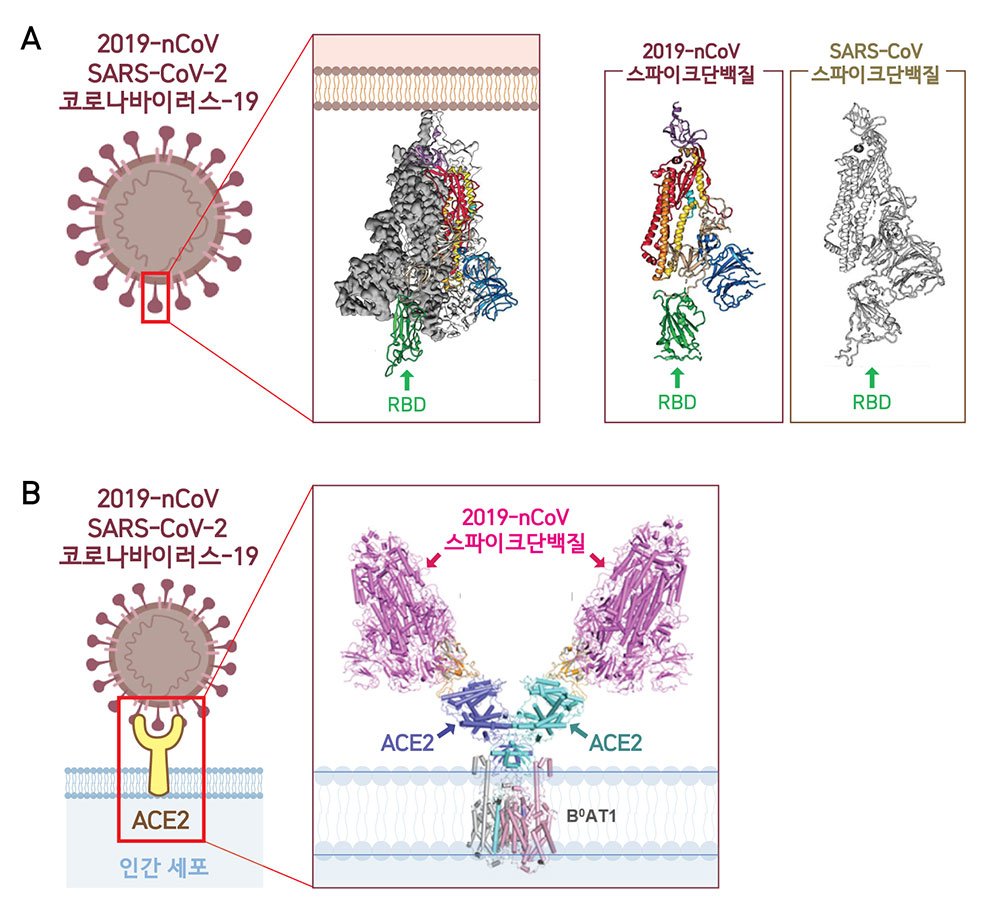
지난 2월 19일 극저온전자현미경(Cryo-EM) 분석을 통해 2019-nCoV의 입체 구조가 밝혀졌다. 3차원 분자구조 분석 결과 2019-nCoV와 사스바이러스의 스파이크단백질이 상당히 비슷한 형태를 가지고 있음이 확인됐다(Walls et al., 2020; Wrapp et al., 2020). 이러한 형태적 유사성 때문에 2019-nCoV 역시 ACE2 수용체를 통해 숙주세포의 표면에 강하게 부착한다는 사실이 밝혀졌고, 스파이크단백질과 ACE2의 결합체의 분자구조도 최근 밝혀졌다(Zhou et al., 2020, Yan et al., 2020).
스파이크단백질을 통한 2019-nCoV와 숙주세포의 결합이 바이러스가 세포에 침투했다는 것을 의미하지는 않는다. 결합 이후 숙주세포에 존재하는 단백질가위가 스파이크단백질의 일부분을 자른 뒤에야 비로소 바이러스가 세포 내로 침투한다. 2019-nCoV의 경우 호흡기세포막에 있는 'TMPRSS2'를 단백질가위로 사용한다는 것이 밝혀졌다(Hoffmann et al., 2020).
향후 자세한 후속연구가 필요하겠지만, 2019-nCoV가 사스바이러스보다 더 빠르게 전염·확산되는 이유도 나왔다. 사스바이러스와 다르게 2019-nCoV가 숙주세포의 ACE2에 더 강하게 결합하고, 스파이크단백질의 일부분이 단백질가위에 의해 더 쉽게 잘라질 수 있도록 변형이 되어 있는 것이 그 원인으로 제시되고 있다.
앞서 설명한 것처럼 코로나바이러스와 숙주세포의 결합은 바이러스 감염의 첫 번째 길목이다. 연구자들은 이 길목을 차단하는 전략을 백신이나 초기 치료제 개발에 활용한다. 미국 제약회사 모더나(Morderna)가 지난 24일 개발했다고 발표한 2019-nCoV 백신 후보물질 mRNA(전령RNA)-1273이 그 사례다.
mRNA-1273 백신은 스파이크단백질의 유전정보를 담은 mRNA를 주사함으로써, 2019-nCoV의 스파이크단백질과 똑같이 생긴 '가짜 스파이크단백질'이 우리 몸에서 스스로 생성되도록 한다. 만들어진 가짜 스파이크단백질을 이용하여 우리 몸속 면역세포들이 바이러스와 싸울 수 있는 항체를 스스로 만들어내는 원리다. 외부에서 가짜 스파이크단백질을 직접 제조해 몸으로 투여할 수도 있지만, 이 경우에는 백신 개발에 더 오랜 기간이 필요하다. 반면, 모더나는 25일 만에 구조설계 및 시험생산까지 완료했고, 올해 4월 임상 1상에 돌입한다고 미국 국립보건원(NIH) 산하 국립알레르기감염병연구소(NIAID)는 밝혔다.
mRNA-1273이 가짜 스파이크단백질을 만든다면, '가짜 수용체'를 만드는 전략도 있다. 중국에서 개발했다고 밝힌 COVID-19의 초기 치료제 후보물질은 '재조합 ACE2'다. 재조합 ACE2는 외부에서 ACE2 수용체를 제작한 뒤 몸속으로 주입하는 원리로 2019-nCoV를 중화한다는 의미에서 중화 단백질의약품으로도 불린다. 이 치료 후보물질은 유입된 바이러스가 재조합 ACE2를 진짜 수용체로 인식하여 결합하도록 만든다. 가짜 수용체와 결합한 바이러스는 자연스레 사멸한다.
사스바이러스와 2019-nCoV의 스파이크단백질 구조가 유사하다는 점에 착안해 기존에 개발되고 있던 사스바이러스 중화 단백질의약품 중 일부를 코로나바이러스-19 치료제로 활용하고자 하는 시도들도 이뤄지고 있다. 국내 연구진(한국화학연구원 CEVI융합연구단)도 최근 이 전략을 제시했다. 연구진은 컴퓨터를 이용한 분자구조 시뮬레이션을 통해 기존 사스 중화항체 2개와 메르스 중화항체 1개가 2019-nCoV와 결합할 수 있을 것으로 예측한 결과를 지난달 27일 학술논문 사전공개 사이트(bioRxiv)에 발표했다(Park et al, 2020).
위에 소개한 백신 및 치료제 개발 사례는 2019-nCoV가 세포 속으로 침투하는 첫 번째 길목을 차단하는 효과적인 전략이다. 하지만 이미 바이러스가 세포 내부로 들어와서 폭발적인 증식이 일어난 경우는 이 전략만으로 역부족이다. 바이러스의 세포 내 증식 원리에 기반을 둔 또 다른 치료전략에 대해서는 다음 리포트에서 다뤄보도록 하겠다.
관련기사
- [IBS 통신]바이러스 변이체 위협적인가?
- [IBS 통신]면역 체계, 돌연변이 방어할 수 있나?
- [IBS 통신]코로나19 백신의 탄생과 패러다임 전환
- [IBS 통신]백신의 종류와 특징
- [IBS 통신]mRNA, 코로나19 백신에서 유전자 치료제까지
- [IBS 통신]코로나19 키워드 'RNA'는 어떤 물질인가
- [IBS 통신]약물 재지정을 통한 코로나19 치료제 발굴:아필리모드
- [IBS 통신]코로나19 항체치료제 개발 어디까지 왔나
- [IBS 통신]자연에서 발견한 코로나19 치료 후보물질
- [IBS 통신]우리집 개와 고양이가 코로나19 옮길 위험 있을까
- [IBS 통신]코로나19 감염여부를 신속·정확하게 진단하는 새로운 방법
- [IBS 통신]코로나 백신 3대 키워드: 안전성, 전달성, 안정성
- [IBS 통신]학부생 인턴, 코로나19 최전선 연구실을 경험하다
- [IBS 통신]코로나19와 정신건강 '마음방역'의 필요성
- [IBS 통신]모더나의 백신 개발, 팀사이언스의 힘
- [IBS 통신]코로나19 수리모델, 방역정책 수립 근거가 되다
- [IBS 통신]코로나19 팬데믹은 기후에도 영향을 미쳤을까
- [IBS 통신]코로나19 초기 감염 병리기전을 밝히다
- [IBS 통신]인체는 코로나19에 어떤 면역반응을 나타내나
- [IBS 통신]국제사회는 허위정보에 어떻게 대처하는가
- [IBS 통신]포스트 코로나와 한국바이러스기초연구소
댓글 정렬