민달희 서울대 교수 "부작용 적고 시술 성공률이 높아"
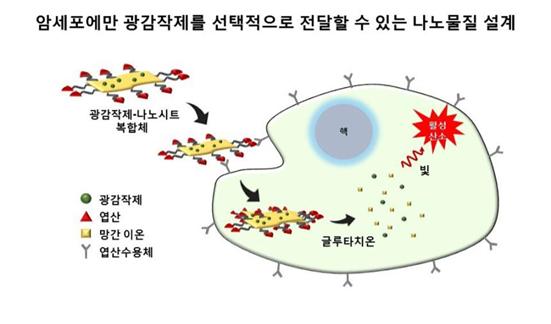
민달희 서울대 교수 연구팀은 빛에 반응하는 화학물질인 광감작제를 활용해 암세포만 골라서 없애는 '2차원 광감작제-나노시트 복합체'를 개발했다고 23일 밝혔다.
기존 반복적인 항암제 투여와 방사선 치료법 등의 항암 치료는 경제적 부담과 전신 부작용을 일으키는 단점이 있다. 광역동치료는 기존 항암 치료와 달리 인체에 무해한 빛을 사용해 국소적인 암세포 치료가 가능하다. 정상세포 손상을 최소화하므로 암치료 새로운 대안으로 주목받고 있다.
광역동치료는 광감작제가 특정 파장대 빛을 흡수해 에너지전달 기작을 거쳐 활성산소를 내 주변 암조직을 손상시켜 치료하는 방법이다.
하지만 광역동치료에 사용되는 핵심 물질인 광감작제는 대부분 물에 잘 녹지 않는 단점이 있다. 투여된 광감작제가 정상조직에도 남기 때문에 햇볕을 쬐면 체내에 잔존한 광감작제에 의해 발생하는 활성산소가 피부를 심각하게 손상시키는 등 부작용을 유발한다.
연구팀은 기존 광역동치료 한계를 극복하기 위해 혈액 내 안정성이 높고 암세포 내 환경에서는 쉽게 분해되는 이산화망간 나노시트에 주목했다. 암세포에만 선택적으로 광감작제를 전달할 수 있는 기능성 나노시트를 개발했다.
연구팀은 암세포에 엽산 수용체가 과다 발현돼 있으므로 엽산을 도포한 나노시트를 사용하면 선택적으로 암세포에만 나노시트가 전달되고 축적이 가능하다는 아이디어를 기반으로 엽산이 도포된 이산화망간 나노시트를 합성했다
먼저 넓은 표면적을 가진 시트 표면에 난용성 광감작제를 효과적으로 적재하고, 체내 투여 시 혈액 내에서 분해나 분리되지 않고 안정성을 유지해 무분별한 광감작제의 방출을 억제했다. 암세포로 들어간 나노시트는 암세포 내에 높은 농도로 존재하는 글루타치온에 의해 완벽하게 분해되면서 적재된 광감작제가 방출되는 것을 종양 동물 모델을 통해 확인했다.
생쥐 실험에서 기존 광감작제 투여량 대비 10%만 혈관 투여해도 뛰어난 항암효과를 보였으며, 암세포 표적 광역동치료 효과를 획기적으로 개선했다.
민달희 교수는 "정상세포 손상을 최소화하면서 암세포만을 표적 치료하는 생체적합적인 2차원 나노시트를 개발한 것"이라며 "부작용이 적고 시술성공률이 높은 차세대 항암치료 기술로 발전시키는데 기여할 것"이라고 말했다.
이번 연구성과는 응용화학 분야 국제학술지인 '투디 머티리얼즈(2D Materials)'에 11자로 게재됐다.
댓글 정렬