허용석 건국대 교수 "암환자 치료 효과 높일 것"
허용석 건국대학교 화학과 교수 연구팀은 면역체계에 의한 암세포 파괴를 방해하는 면역 체크포인트 단백질과 면역항암제들의 복합체 결정 구조를 규명해 '면역항암제 작동 메커니즘'을 제시했다고 6일 밝혔다.
암세포는 일반 정상세포와 달리 면역세포인 T세포에 의해 인식되고 파괴된다. 하지만 암세포는 면역 체크포인트 단백질을 이용해 T세포의 공격을 회피할 수 있다.
면역 체크포인트 단백질에는 PD-1, PD-L1, CTLA-4 등이 있다. 이들이 서로 결합하면 암세포가 T세포의 공격을 피하기 위해 암세포가 아닌 것처럼 속이는 것이다.
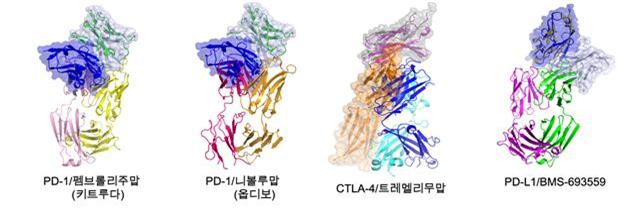
암세포의 PD-L1이 T세포의 PD-1과 결합하면 T세포에게 암세포를 공격하지 말라는 면역회피 신호를 보낸다. 그러나 투여된 면역 항암제가 PD-L1과 PD-1의 결합부위에 미리 달라붙어 면역회피 신호를 차단시킨다. 면역회피 신호를 받지 않은 T세포는 암세포를 제거하게 된다.
면역항암제가 T세포의 CTLA-4에 결합하면 암세포와 T세포가 접근할 수 없게 돼 면역학적 시냅스가 형성되지 못한다. 면역회피 신호를 받지 않은 T세포가 암세포를 파괴하는 것이다.
허용석 교수는 "이번 성과는 면역항암제 효능을 개선시키기 위한 중요한 분자 구조적 정보를 제공한다"며 "결합 부위와 결합 방식이 서로 다른 면역항암제들을 조합해 암환자들의 치료 효과를 높일 수 있을 것"이라고 연구의 의의를 말했다.
이번 연구성과는 '네이처 커뮤니케이션즈'(Nature Communications)에 지난달 31일 자로 게재됐다.
댓글 정렬